Гормон роста: польза или вред
Содержание:
- Гормон роста поддельный
- Механизм действия
- Отношение IGF-1 к общему состоянию здоровья и долголетию
- Разработка опытно-промышленной технологии выделения и очистки рГРЧ
- Повышение производительности
- ГР и ИФР-1: мутации, делающие жизнь длиннее
- Как правильно расшифровать результаты анализа
- Проявления акромегалии:
- Разработка методов контроля и создание стандарта качества на субстанцию рГРЧ
- История
- Разница между гормоном роста и ИФР-1
- Влияние гормона роста на организм
- Как повысить уровень соматотропина без инъекций
- В каких случаях нужно сдавать анализы на гормоны
- Список литературы
- Доклинические и клинические испытания рГРЧ
- Что такое гормон роста
- Что включает в себя подготовка
Гормон роста поддельный
Практически не прекращаются споры о поддельности того или иного препарата гормона роста. Особенно много таких споров ведется вокруг препарата Jintropin производства китайской GenSci. Попробуем в очередной раз «отделить зерна от плевел».
Гормон роста в виде порошка (в нерастворенном состоянии) должен храниться преимущественно в холодильнике. В растворенном виде – ТОЛЬКО в холодильнике и то не больше недели. При температуре, превышающей 18-20°С, гормон роста в порошке начинает медленно, но верно разрушаться («умирать»). Иногда вы приобретаете совершенно разрушенный («мертвый») гормон роста, иногда такой, действенность которого существенно понижена.
В случае Jintropin’а от такого разрушения защищает термоизолирующая упаковка, хотя и она не дает абсолютной гарантии. Но покупка препаратов без такой упаковки с рук (будь то Jintropin или другой препарат) крайне нежелательна – вы не можете знать наверняка, где и как хранился препарат, даже если ваш «дилер» будет давать все органы на отсечение, что условия хранения строго соблюдались. Даже покупка препарата в аптеке не дает стопроцентной гарантии, что он сохранил всю свою силу – в аптечную сеть гормон роста может попадать, пройдя «все круги ада» и провалявшись на различных складах много месяцев.
Были отмечены случаи появления на рынке контрафактного варианта Jintropin’а. Однако фальсификаторам удается имитировать только флакон с наклейкой, изготовить флакон с керамическим нанесением надписи оказывается экономически невыгодным. Содержимое фальсификата, по отзывам, ничего общего с синтетическим гормоном роста не имеет. В лучшем случае, это просто плацебо. Надо отметить, что далеко не все флаконы с наклейкой являются фальсификатом. Но дабы не испытывать судьбу при приобретении довольно дорогостоящего продукта стоит, все же, отдать предпочтение флаконам с керамическим нанесением информации.
Механизм действия
IGF-1 является первичным медиатором действия гормона роста (GH). Гормон роста вырабатывается передней долей гипофиза , попадает в кровоток и затем стимулирует печень к выработке IGF-1. Затем IGF-1 стимулирует системный рост организма и оказывает стимулирующее воздействие на почти все клетки тела, особенно на скелетные мышцы , хрящи , кости , печень , почки , нервы , кожу , кроветворные и легочные клетки. Помимо инсулиноподобных эффектов, IGF-1 также может регулировать синтез клеточной ДНК .
IGF-1 связывается с по меньшей мере , две поверхности клеток рецепторных тирозинкиназ : The ИФР-1 — рецептора (IGF1R) и рецептора инсулина . Его основное действие опосредовано связыванием со специфическим рецептором IGF1R, который присутствует на поверхности многих типов клеток во многих тканях. Связывание с IGF1R инициирует внутриклеточную передачу сигналов. IGF-1 является одним из наиболее мощных природных активаторов сигнального пути AKT , стимулятором роста и пролиферации клеток и мощным ингибитором запрограммированной гибели клеток . Рецептор IGF-1, по-видимому, является «физиологическим» рецептором, потому что он связывает IGF-1 со значительно более высоким сродством, чем рецептор инсулина. IGF-1 активирует рецептор инсулина примерно в 0,1 раза сильнее, чем инсулин. Часть этой передачи сигналов может происходить через гетеродимеры IGF1R / рецептора инсулина (причина путаницы в том, что исследования связывания показывают, что IGF1 связывает рецептор инсулина в 100 раз хуже, чем инсулин, но это не коррелирует с фактической эффективностью IGF1 in vivo. при индуцировании фосфорилирования рецептора инсулина и гипогликемии).
IGF-1 связывает и активирует свой собственный рецептор IGF-1R посредством экспрессии на клеточной поверхности рецепторных тирозинкиназ (RTK) и дальнейшего сигнала через многочисленные каскады внутриклеточной трансдукции. IGF-1R является важнейшим ролевым индуктором в модуляции метаболических эффектов IGF-1 на клеточное старение и выживаемость. В локализованной клетке-мишени IGF-1R опосредует паракринную активность. После его активации происходит инициация внутриклеточной передачи сигналов, вызывая множество сигнальных путей. Важный механистический путь, участвующий в посредничестве каскада, влияет на ключевой путь, регулируемый фосфатидилинозитол-3 киназой ( PI3K ) и ее нижележащим партнером, mTOR (мишень рапамицина млекопитающих). Рапамицин связывается с ферментом FKBPP12, подавляя комплекс mTORC1. mTORC2 остается незатронутым и реагирует повышающим регулированием AKT, управляя сигналами через ингибированный mTORC1. Фосфорилирование эукариотического фактора инициации трансляции 4E ( EIF4E ) с помощью mTOR подавляет способность эукариотического фактора инициации трансляции 4E-связывающего белка 1 ( EIF4EBP1 ) ингибировать EIF4E и замедлять метаболизм. Мутация сигнального пути PI3K-AKT-mTOR является важным фактором образования опухолей, обнаруживаемых преимущественно на коже, внутренних органах и вторичных лимфатических узлах (саркома Капоши). IGF-1R позволяет активировать эти сигнальные пути и впоследствии регулирует клеточное долголетие и метаболический повторный захват биогенных веществ. Терапевтический подход, направленный на уменьшение таких скоплений опухолей, может быть вызван ганитумабом. Ганитумаб представляет собой моноклональное антитело (mAb), антагонистически направленное против IGF-1R. Ганитумаб связывается с IGF-1R, предотвращая связывание IGF-1 и последующий запуск сигнального пути PI3K-mTOR; ингибирование этого пути выживания может привести к подавлению роста опухолевых клеток и индукции апоптоза опухолевых клеток.
Инсулиноподобный фактор роста 1 , как было показано , связываются и взаимодействуют со всеми семь IGF-1 связывающих белков (БСИФР): IGFBP1 , IGFBP2 , IGFBP3 , IGFBP4 , IGFBP5 , IGFBP6 и IGFBP7 . Некоторые IGFBP ингибируют. Например, и IGFBP-2, и IGFBP-5 связывают IGF-1 с более высоким сродством, чем он связывает свой рецептор. Следовательно, повышение уровней этих двух IGFBP в сыворотке приводит к снижению активности IGF-1.
Отношение IGF-1 к общему состоянию здоровья и долголетию
В некоторых организмах, например, таких, как плодовые мушки, черви и крысы инсулиноподобный фактор роста IGF-1 включается в управление продолжительностью жизни.
В большинстве исследований на мышах, блокировка пути гормона роста / IGF-1 приводит к увеличению продолжительности жизни (до 55%). Однако, у людей, прямой связи между уровнем IGF-1 и продолжительностью жизни обнаружено не было. {}
Несколько популяционных исследований, описывающих связь между IGF-1 и риском смерти, были опубликованы с противоречивыми результатами. Два исследования показали повышенный риск, связанный с более высокий уровнем IGF-1, в то время как три показали повышенный риск при низких значениях IGF-1. И в шести исследованиях не было четкой ассоциации. {}
Однако, в целом, низкие или высокие уровни IGF-1 увеличивают риск смерти от всех причин. {И}
В Мета-анализе двенадцати исследований, проведенного в 2011 году с 14,906 участниками, риск смерти от всех причин был увеличен у пациентов с низким, а также высоким уровнем IGF-1. {И} Люди с низкими показателями IGF-1 демонстрировали рост на 27% риска смерти от всех причин, а люди с более высокими уровнями проявляли повышенный риск смерти на 18%.
Эти результаты говоря нам, что низкие уровни IGF-1 являются более значительной проблемой, чем высокие уровни IGF-1, но лучше, если показатели этого гормона будут сбалансированы. {И}
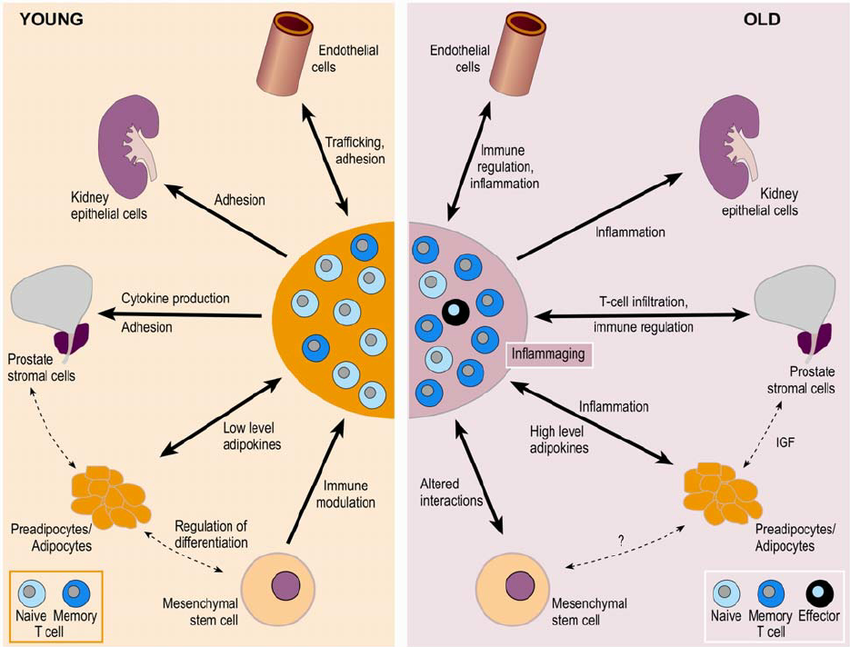 Влияние инсулиноподобного фактора роста (соматомедина-С) на различные органы при молодом и старшем возрасте.
Влияние инсулиноподобного фактора роста (соматомедина-С) на различные органы при молодом и старшем возрасте.
Уровни гормона IGF-1 после пика во время развития детского организма нормализуются и находятся в примерно одинаковых показателях до 40 лет. Затем значения IGF-1 начинают медленно снижаться.
Когда человек имеет установленный онкологический диагноз, то, вероятно, будет лучше, если показатели инсулиноподобного фактора роста IGF-1 будут понижены, но не слишком низки.
Если человек болен аутоиммунным заболеванием или у него есть постоянное хроническое воспаление, например, при ожирении, то, вероятно, будет лучше, если показатели IGF-1 будут повышены, но не слишком высоко.
Разработка опытно-промышленной технологии выделения и очистки рГРЧ
Создание стабильного высокопроизводительного штамма — продуцента соматотропина и разработка технологии его культивирования позволили разработать опытно-промышленную технологию получения фармакопейной субстанции рГРЧ из ТВ. Как уже было отмечено выше, одной из основных задач исследования было максимально полно использовать накопленный опыт по созданию технологии выделения и очистки субстанции генноинженерного инсулина человека, в том числе и аппаратурного оформления процесса, на тех стадиях, на которых это позволяет коэффициент масштабирования.
Процесс получения субстанции соматотропина состоит из трех основных этапов: получения рекомбинантного белка (РБ) — Met-соматотропина в мономерной форме (включая восстановление и ре- натурацию РБ с последующей его очисткой), получения рГРЧ из РБ ферментативным отщеплением N-концевого аминокислотного остатка метионина и очистки соматотропина с получением фармакопейной субстанции. Технологическая схема получения субстанции рГРЧ представлена на рис. 3.
Были проведены 20-кратное масштабирование процесса ферментации штамма-продуцента и оптимизация процессов рефолдинга и очистки. В ходе рефолдинга применялось аппаратурное оформление процесса, ранее разработанное для технологии производства инсулина. Перед этой стадией обессоливали раствор денатурированного рГРЧ на колонке с сефадексом G-25 для удаления денатурирующего агента.
Ферментативное отделение N-концевого аминокислотного остатка метионина производили под действием лейциновой аминопептидазы Aeromonas proteolitica, как это было описано выше, но время реакции было значительно уменьшено для снижения уровня образования побочных продуктов. Выход на стадии достигал 82%.
Для последующей очистки рГРЧ был использован декстрановый сорбент с привитыми группами С4, н-пропанол заменили на более экономичный и менее токсичный этанол. В результате получили рГРЧ фармакопейной чистоты по основным показателям нормативной документации. Выход на стадии составил 79%.
На завершающей стадии получения субстанции рГРЧ использовали гель-фильтрацию, отделяя препарат от номинируемых низко- и высокомолекулярных примесей и переводя рГРЧ в фармакопейный раствор. Выход составлял около 96%, содержание номинируемых примесей соответствовало требованиям Фармакопейной статьи предприятия (ФСП).
Повышение производительности
Первым описанием использования GH в качестве допингового агента был «Справочник по подпольным стероидам» Дэна Дюшена, вышедший в Калифорнии в 1982 году; неизвестно, где и когда GH впервые был использован таким образом.
Спортсмены, занимающиеся многими видами спорта, использовали гормон роста человека, чтобы попытаться улучшить свои спортивные результаты. Некоторые недавние исследования не смогли подтвердить утверждения о том, что гормон роста человека может улучшить спортивные результаты профессиональных спортсменов-мужчин. Многие спортивные общества запрещают использование GH и вводят санкции против спортсменов, уличенных в его использовании. Однако, поскольку GH является мощным эндогенным белком, очень трудно обнаружить допинг GH. В Соединенных Штатах GH официально доступен только по рецепту врача.
ГР и ИФР-1: мутации, делающие жизнь длиннее

- За последние 4 года был выявлен широкий спектр мутаций, связанных с ГР, которые увеличивают продолжительность жизни мышей:
- снижение количества свободного ИФР-1 и его посредников,
- снижение числа субстратов инсулинового рецептора – 1 и 2 (СИР-1,2) и посредников инсулина,
- дефицит соматолиберина,
- прекращение производства S6-киназы, приводящее к уменьшению количества белков mTOR (ранее было показано, что применение рапамицина, ингибитора mTOR, увеличивает продолжительность жизни у мышей).
- Мутации, затрагивающие «нижние звенья» оси влияния ГР (ИФР-1, рецептор ИФР-1, посредники ИФР-1 и инсулина и т.д.) слабее влияли на продолжительность жизни, чем нарушения, напрямую касавшиеся синтеза и функций самого ГР.
- Некоторые мутации ИФР-1 увеличивали продолжительность жизни только у самок. Это было подтверждено в опытах на мышах и собаках.
- Выработка ИФР-1 в некоторых органах не зависит от ГР, поэтому исключение влияния ГР не препятствует работе ИФР-1 в мозге и сердце, но снижает его концентрацию в циркулирующей крови, таким образом защищая животных от рака.
- Один из предположительных механизмов влияния ГР на продолжительность жизни – это регуляция чувствительности к инсулину.
- ГР является контринсулярным гормоном и увеличивает инсулинорезистентность
- ИФР-1 повышает чувствительность тканей к инсулину.
- Ожидаемая положительная корреляция между количеством циркулирующего ИФР-1 и размером тела взрослой особи наблюдалась – однако, только внутри вида. При сравнительном анализе 36 различных видов животных, от мышей до полярных медведей, было установлено, что уровень ИФР-1 у более крупных видов ниже, чем у мелких.
Как правильно расшифровать результаты анализа
Анализ крови на соматотропный гормон в норме должен предоставлять следующие показатели:
- 2-15 нг/мл у женщин;
- 2-10 нг/мл у мужчин.
Отклонения от нормы в результатах анализа могут свидетельствовать о следующих проблемах у пациента.
- Повышенная концентрация в крови человека гормона роста может обнаруживаться в случаях нарушения питания организма, опухолях легких, желудка, акромегалии, карликовости, гипофизарного гигантизма. К увеличению данной цифры может привести продолжительный отказ от пищи, избыточная физическая активность пациента. Этот результат исследования также возможен при анорексии неврогенного характера, циррозе печени, неуправляемом сахарном диабете, почечной недостаточности.
- Пониженная концентрация гормона роста в крови, которая выявляется при проведении анализа, может присутствовать как результат гипопитуаризма, избыточной функции коры надпочечников, гипофизарном нанизме. Также показатель данного вещества может снизиться после влияния радиации, проведения химиотерапии.
Результаты исследования могут рассказать о наличии у пациента опухоли гипоталамуса, гипофиза, дают возможность обнаружить сокращение работы щитовидки и гипофиза. Также с его помощью можно отличить акромегалию от гигантизма, отслеживать результативность лечения соматотропным гормоном.
Проявления акромегалии:

— увеличение размера кистей и стоп. Старые кольца и перчатки становятся малы, обувь тесна.
— черты лица становятся более грубыми и крупными — увеличивается нос, более выраженными становятся надбровные дуги, нижняя челюсть больше выступает вперед, губы утолщаются. Расширяется промежуток между передними верхними зубами (диастема).
— потливость,
— повышенная жирность кожи, утолщение кожи,
— боли в суставах,
— часто развивается синдром карпального канала, проявляющийся онемением нескольких пальцев на руке, ползанием мурашек, болью,
— узлы в щитовидной железе,
— повышение сахара крови вплоть до развития сахарного диабета,
— повышение холестерина крови за счет «плохого»,
— выделение капель молока из молочных желез,
— повышение артериального давления,
— аритмия,
— нарушение дыхания во сне (остановки дыхание различной продолжительности)
— опухоли кишечника, желудка.
— головные боли,
— при больших размерах опухоли гипофиза могут быть нарушения зрения.
— у женщин — нарушение менструального цикла,
— утомляемость, сонливость.
Разработка методов контроля и создание стандарта качества на субстанцию рГРЧ
В соответствии с отечественными и международными требованиями к производству лекарственных препаратов в ходе наших дальнейших исследований был разработан стандарт качества на субстанцию рГРЧ — ФСП 42-0549-5553-04 — «Соматотропин человеческий», 2004 г.
Характеристики, заложенные в национальный стандарт качества рГРЧ, непринципиально отличаются от таковых для субстанции инсулина, поскольку и тот и другой препарат создан на основе методов рекомбинантных ДНК, и характер номинируемых примесей отличается незначительно и определяется в основном физико-химическими свойствами соответствующих белков.
В табл. 2 приведены некоторые показатели качества созданного нами национального стандарта субстанции рГРЧ в сравнении с требованиями Британской фармакопеи.
Из табл. 2 видно, что субстанция соматотропина, так же как и АФС других генно-инженерных белков, должна быть охарактеризована качественно и количественно (показатели «подлинность» и «количественное определение»). Для определения первого показателя дополнительно используется метод ионообменной ВЭЖХ, а биологические методы не применяются. Количественное определение проводится методом эксклюзионной ВЭЖХ.
Так же хроматографически определяют родственные белки, в основном различные дезамидированные формы рГРЧ, высокомолекулярные примеси — димеры и полимеры соматотропина, расщепленную форму гормона. Примеси, номинируемые этими показателями, могут образовываться как при нарушении технологического процесса производства субстанции, так и при ее хранении.
Характерными для генно-инженерных фармацевтических белков показателями качества субстанции соматотропина являются содержание иммунореактивных примесей и содержание ДНК клеток штамма-продуцента. Для определения иммунореактивных примесей нами был разработан и внедрен метод твердофазного иммуноферментного анализа. Содержание иммунореактивных примесей не должно превышать 3 нг/мг соматотропина.
Остаточную ДНК штамма-продуцента определяют с помощью метода гибридизации, для чего используют биотинилированную ДНК клеток хозяина и ее реакцию взаимодействия с конъюгатом стрептавидина и щелочной фосфатазы. Содержание остаточной ДНК не должно превышать 10 пг/мг рГРЧ.
История
Первый гормон роста человека, предназначенный для медицинского использования, был извлечен из экстрактов гипофиза человеческого происхождения. Такие препараты обычно называются кадаверными (трупными) препаратами гормона роста. Из каждого трупа может быть извлечено приблизительно 1 мг ГРЧ (дозирование 1 раз в день).
Первое успешное лечение человеческим кадаверным ГР датировано 1958 годом. Вскоре после этого эти лекарственные средства были представлены на рынок, и продавались в США до 1985 года.
FDA запретило их продажу в этом году, после того, как было доказано, что их применение может быть связано с развитием болезни Крейтцфельдта-Якоба (БКЯ), высокодегенеративного и в конечном итоге фатального заболевания мозга. Болезнь может передаваться от одного человека к другому при исключительных обстоятельствах (обычно при переливании крови или имплантации органа), и, скорее всего, инициируется извлечением чГР из инфицированных трупов. БКЯ имеет очень медленный инкубационный период и заболевание было диагностировано после 4-30 лет лечения кадаверным гормоном роста. По оценкам 2004 года, по меньшей мере 26 пациентов, принимавших кадаверный ГР в Соединенных Штатах, страдали этим заболеванием. Общая заболеваемость, таким образом, составила менее 1%, поскольку известно, что данный препарат принимало приблизительно 6000 пациентов.
В 1985 году FDA одобрило первый синтетический препарат человеческого гормона роста. Он является первым доступным синтетическим препаратом гормона роста в мире, производящимся при помощи процесса, называемого Inclusion Body Technology. Эта технология включает в себя вставку ДНК, кодирующего белок ЧГР, в бактерии кишечной палочки (E.coli), которые собирают и синтезируют чистый белок. В результате синтеза производится чистый гормон без биологических загрязнений, что устраняет возможность передачи БКЯ. Одобренный препарат получил название somatrem (Protropin), и был основан на производственной технологии, разработанной компанией Genentech в 1979 году. Somatrem разработали вовремя, так как трупный ГР был изъят с рынка в этом же году. Этот гормон фактически является немного отличным от чГР белка, однако отображает биологические свойства природного гормона. Protropin изначально был весьма успешным синтетическим продуктом ГР. К 1987 году, однако, Kabi Vitrum (Швеция) опубликовала методы производства чистого синтетического соматотропина с точной аминокислотной последовательностью эндогенного гормона роста. Было также обнаружено, что неестественная структура Somatrem вызывает гораздо более высокий процент реакций на антитела у больных, что может уменьшить эффективность препарата.
Соматропин рассматривается как более надежный препарат, и препарат сохраняет за собой лидерство продаж ГРЧ по всему миру.
Разница между гормоном роста и ИФР-1
Гормон роста влияет на синтез белка и рост мышечных волокон (а также связок, хрящей, костной ткани, внутренних органов) опосредствованно. Но – все через тот же инсулиноподобный фактор роста, синтезируемый под влиянием ГР в печени. Является ли он идентичным по действию тому рекомбинантному ИФР-1, который мы вводим в организм извне – большой вопрос. Скорее всего, нет. Является ли синтезируемый печенью IGF-1 идентичным по действию тому фактору роста, который образуется в клетках мышц, тоже вопрос. И ответ на него тоже, скорее всего, будет отрицательным. Гормон роста способен продлить период полужизни ИФР-1, но так ли это необходимо в случае и так достаточно «долгоживущего» Long R3 IGF-1, по крайней мере, если речь идет о наборе мышечной массы (о сжигании жира мы уже говорили несколько выше)? Возможно, продление периода полужизни инсулиноподобного фактора роста сверх необходимой меры сулит в этом плане больше отрицательных перспектив, нежели положительных, что пока что, кстати, подтверждается практикой.
Инсулиноподобный фактор роста может применяться и сам по себе (хотя показатели роста мышечной массы под влиянием ИФР-1 лежат в очень широких пределах – от совершенно ничтожных до выдающихся; при этом речь идет именно о «сухой» мышечной массе), а гормон роста требует для эффективной работы применения андрогенов. С другой стороны, показатели роста мышечной массы под влиянием комбинации андрогенов и гормона роста куда более стабильны. Кстати, недавний эксперимент, результаты которого изложены в статье «Geriatric Growth Hormone Interventions Not Ready For Clinical Use» (Journal Of the American Medical Association, 2002), показал, что пожилые люди могут добиваться прироста мышечной массы (существенного – до 3 кг за 26 недель) и при применении гормона роста «соло». Но возраст участников эксперимента составлял 65-88 лет, то есть, секреция собственного ГР у каждого из них была куда ниже нормы.
Влияние гормона роста на организм
Для мужчин, занимающихся бодибилдингом, наибольший интерес представляет анаболическое действие соматотропина. Гормон вызывает активный рост мышц, позволяя добиться желаемого рельефа и объема. В то же время он ускоряет заживление ран, что снижает травматизм при спортивных тренировках, способствует уменьшению жировых отложений. Весомым плюсом для культуристов является антикатаболическое действие соматотропина, тормозящее разрушение мышц.
И это не единственные полезные свойства гормона, поскольку он:
- обладает омолаживающим эффектом;
- регулирует процессы распределения энергии;
- стимулирует рост внутренних органов, компенсируя их возрастную атрофию;
- увеличивает уровень глюкозы в крови, укрепляет иммунитет;
- способствует приросту и укреплению костной ткани (при приеме до 26 лет).
Примечательно, что первые препараты соматотропина делали на основе вытяжки из гипофиза трупов, и только с 1981 года их начали производить синтетическим способом. В профессиональном спорте использование соматотропного гормона запрещено, однако в бодибилдинге он активно применяется мужчинами для наращивания мышечной массы. Стоит учитывать, что росту силовых показателей СТГ не способствует, поэтому принимать его в пауэрлифтинге как средство повышения производительности бессмысленно. Не влияет он и на выносливость.
Как повысить уровень соматотропина без инъекций
Неразумное употребление гормона роста может привести к нарушению пищеварения, болезням печени или почек, поражению щитовидной железы. Желая сохранить молодость кожи и стройность фигуры, откажитесь от БАДов в пользу простых и эффективных методов увеличения уровня соматотропина.
Здоровый сон
Соматотропин наиболее активно вырабатывается во время ночного отдыха. Для поддержания гормона в крови гипофизу требуется не менее 7–8 часов полноценного сна. Старайтесь высыпаться, откажитесь от вечернего просмотра фильмов, не сидите в гаджетах.
Занимайтесь спортом
При регулярной физической нагрузке ускоряется синтез соматотропина: организм потребляет больше калорий, поэтому гипофиз старается восполнить их недостаток, быстрее расщепляя жиры. Занимайтесь не менее 30 минут 5 раз в неделю, регулярно бегайте по утрам, ведите более активный образ жизни.
Контрастные обливания
При смене температур организм испытывает стресс, включаются защитные реакции, и активируется работа всех систем. В числе прочих гормонов усиленно вырабатывается соматотропин, ускоряя расщепление белков и углеводов. Приучайте себя к контрастному утреннему душу, чтобы сохранить бодрость и активность в течение рабочего дня. Начните с постепенного снижения температуры в течение 5 секунд, постепенно доводите до 20 секунд.
Витамины и питание
Для увеличения синтеза гормона роста важно поддерживать высокий показатель витаминов С и Е.
Принимайте добавку ГАМК. Гамма-аминомасляная кислота (ГАМК) — это непротеиногенная аминокислота, которая действует как нейротрансмиттер, посылая сигналы в ваш мозг.
Как хорошо известное успокаивающее средство для мозга и центральной нервной системы, он часто используется для улучшения сна. Интересно, что это также может помочь повысить уровень гормона роста.
Одно исследование показало, что прием добавки ГАМК приводит к увеличению HGH на 400% в покое и на 200% после упражнений.
ГАМК также может повысить уровень гормона роста за счет улучшения сна, поскольку высвобождение гормона роста в ночное время связано с качеством и глубиной сна.
Важно правильно питаться, чтобы соматотропин расщеплял жиры более активно. Постарайтесь чаще употреблять рыбу, обогащенную Омега-3 и Омега-6, авокадо, орехи
В зимнее время применяйте БАДы, содержащие аргинин, лизиновую и глутаминовую кислоты.
Придерживаясь перечисленных советов, вы заметите, что через несколько недель повысится активность, выносливость при выполнении физических нагрузок. При усиленной выработке соматотропина кожа станет более упругой и подтянутой, словно сияя изнутри здоровьем. опубликовано econet.ru
Подборка видео МАТРИЦА ЗДОРОВЬЯ https://course.econet.ru/live-basket-privat в нашем закрытом клубе
P.S. И помните, всего лишь изменяя свое потребление — мы вместе изменяем мир! econet
В каких случаях нужно сдавать анализы на гормоны
Если баланс эндокринной системы нарушается, в организме развиваются изменения. Нередко достаточно предельно малых отклонений от нормы, чтобы запустить патологический процесс.
Достаточно долго такие патпроцессы могут протекать бессимптомно. Когда же появляется симптоматика, то нередко патогенез уже необратим. Чтобы выявлять бессимптомные гормональные нарушения на ранних стадиях современная доказательная медицина настоятельно рекомендует пакетные проверки. Один раз в 6-12 месяцев достаточно сдать кровь на анализ, чтобы оценить состояние эндокринной системы и не допустить развития гормональных заболеваний.
Кроме этого, о необходимости сдать анализ на гормоны может свидетельствовать ряд признаков:
- увеличение массы тела;
- бесплодие;
- нарушение функций внутренних органов;
- расстройства либидо;
- подозрение на наличие новообразований;
- избыточный рост волос на лице или теле;
- угревая болезнь;
- нарушения менструального цикла у женщин.
Также обязательно контролировать уровень гормонов при беременности, чтобы не допустить аномалий развития плода.
При планировании беременности необходимо пройти обследование щитовидной железы: сделать УЗИ щитовидной железы, пройти исследования гормонов ТТГ, Т4 свободный (свободный тироксин) и АТ к ТПО (антитела к тиреопероксидазе)
Во время беременности, если есть нарушение функций щитовидной железы, необходимо 1 раз в триместр проводить скрининг гормона ТТГ и консультироваться у эндокринолога.
При запущенных нарушениях баланса гормонов в организме развиваются системные изменения вплоть до инвалидности.
Список литературы
1. Дедов И. И., Тюльпаков А. Н., Петеркова В. А. Соматотропная недостаточность. — М , 1998.
2. Дедов И. И., Петеркова В. А., Безлепкина О. Б., Нагаева Е. В. Атлас. Соматотропная недостаточность у взрослых. -М., 2004.
3. Диагностика и лечение соматотропной недостаточности у детей. Национальный консенсус. — М., 2005. — С. 1-5.
4. Bannik Е. M., Raat Н. et al. // J. Pediatr. — 2006. — Vol. 148, N 1.-Р. 95-101.
5. Bowlby D. А., Rapaport R. // Pediatr. Endocrinol. Rev. — 2004. — Suppl. 1. — P. 68-77.
6. Bramswig J. H. // Endocrine. — 2001. — Vol. 15, N1. — P. 5-13.
7. Cuneo R. С. et al. // J. Clin. Endocrinol. Metab. — 1998. — Vol. 83.-P. 107-116.
8. Cufield W. S., Lindberg A. et al. // Horm. Res. — 2006. — Vol. 65. — Suppt. 3. — P. 153-159.
9. D’Amico S., Shi J. et al. // Am. J. Clin. Nutr. — 2006. — Vol. 84, N 1. -P. 204-211.
10. Fuqua J. S. // Semin. Pediatr. Surg. — 2006. — Vol. 15, N 3. -P. 162-169.
11. GH Research Society. Consensus guidelines for the diagnosis and treatment of growth hormone (GH) deficiency in childhood and adolescence: summary statement of the GH Research Society // J. Clin. Endocrinol. Metab. — 2000. — Vol. 85. — P. 3990-3993.
12. Koltowska-Haggstrom M. et al. // Eur. J. Endocrinol. — 2006. -Vol. 155, N l.-P. 109-119.
13. Lindholm J. // Pituitary. — 2006. — Vol. 9, N 1. — P. 5-10.
14. Macario M. E. et al. // Br. Med. J. — 1991. — Vol. 302. — P. 1149.
15. Magiakou M. A. // Pediatr. Endocrinol. Rev. — 2004. — Suppl. 3. — P. 484-489.
16. Mahan J. D. et al. // Pediatr. Nephorol. — 2006. — Vol. 21, N 7. — P. 917-930.
17. Myers S. E. et al. // J. Pediatr. — 2000. — Vol. 137. — P. 42- 49.
18. Park E., Bailey J. D., Cowell С. А. // Pediatr. Res. — 1983.- Vol. 17. — P. 1-7.
19. Schambelan M. et al. // Ann. Intern. Med. — 1996. — Vol. 125. — P. 873-882.
20. Sizonenko P. C., Clayton P. E., Cohen P. et al. // Growth Horm. IGF Res. — 2001. — Vol. 11, N 3. — P. 137-165.
21. Van den Broeck J., Van Teunenbroek A., Hokken-Koelega A. et al. // J. Pediatr. Endocrinol. Metab. — 1999. — Vol. 12. — P. 673-676.
22. Waters D. et al. // Ann. Intern. Med. — 1996. — Vol. 125. — P. 865-872.
Доклинические и клинические испытания рГРЧ
Доклинические испытания включали в себя исследования острой и субхронической токсичности, а также доклинической эффективности, которые показали, что препарат «Растан» не отличается от зарегистрированного в РФ препарата «Генотро- пин» (Pharmacia&Upjohn) по активности и безопасности у животных.
Изучение клинической эффективности и безопасности препарата «Растан» проводилось под руководством проф. В. А. Петерковой в Институте детской эндокринологии Эндокринологического научного центра РАМН — ЭНЦ РАМН (дир. — акад. И. И. Дедов). Полученные в ходе исследования данные позволяют судить о высокой эффективности и безопасности препарата «Растан», не уступающих зарубежным аналогам.
Что такое гормон роста
Гормон роста человека (ГРЧ) – это белковое соединение, вырабатываемое частью головного мозга, известной как гипофиз. Производство этого вещества зависит от других гормонов, продуцируемых в гипоталамусе, а также в желудочно-кишечном тракте и поджелудочной железе. После того как гипофиз выдаст очередную порцию ГРЧ, это вещество остается активным в кровотоке всего несколько минут. Но этого времени достаточно, чтобы печень преобразовала его в факторы роста, наиболее важным среди которых является инсулиноподобный фактор роста-1, который, собственно, и наделяет разные клетки способностью к росту.
Гипофиз выбрасывает ГРЧ в определенных условиях. Например, после интенсивной физической нагрузки, после травмы, а также во время сна. В организме здорового человека гормон роста интенсивнее производится в ночное время. Также меняется активность этого процесса и в разном возрасте. У детей, например, выработка гормона происходит довольно интенсивно, достигая своего пика в период полового созревания, благодаря чему дети быстро растут и развиваются. Но уже в среднем возрасте активность гипофиза замедляется, и количество продуцируемого ГРЧ снижается.
Что включает в себя подготовка
Подготовка к сдаче анализа крови на гормон роста очень проста, от пациента требуется всего лишь скрупулезное соблюдение следующих несложных правил. Итак, перед анализами необходимо выполнить следующие требования.
- Если приблизительно за 3-5 суток до анализа крови пациент подвергался рентгенологическому или ультразвуковому исследованию, сканированию, другим медицинским манипуляциям, обязательно нужно поставить лечащего врача в известность об этом.
- Перед проведением исследования нужно внимательнее относиться к своему ежедневному меню. В частности приблизительно за 5 суток до проведения анализов на гормон роста желательно не употреблять жареную, жирную еду.
- Крайне желателен также отказ от всех лечебных препаратов, которые могут привести к искажению результатов расшифровки анализа. Разумеется, это возможно не всегда, но тогда нужно уведомить доктора об этом. Исключением является ситуация, когда исследование проводится для проверки эффективности лечения. В этом случае прекратить прием назначенных врачом препаратов нужно в день анализа. Увеличение концентрации в крови соматотропного вещества вполне может стать итогом приема таких препаратов как бромкриптин, глюканом, клонидин, эстроген, инсулин, адренокортикотропный гормон, оральные контрацептивы и так далее. В идеале любой препарат, если его прием невозможно приостановить, следует обсудить с врачом.
- За трое суток до проведения анализа крови на гормоны категорически запрещается употреблять спиртные напитки. От сигарет желательно отказаться хотя бы в день проведения исследования (чем раньше, тем лучше).
- За 12 часов до процедуры сдачи анализа крови можно употреблять исключительно чистую воду, так как манипуляция должна осуществляться натощак. Также запрещено употребление любых других напитков – чая, кофе, минеральной воды, сока.
- Снизить качество результатов анализов могут также и чрезмерные физические нагрузки. Примерно за три дня до проведения сдачи крови на исследования лучше начать воздерживаться от физических упражнений, занятий любыми видами спорта.
Если анализ крови на гормон роста проводится повторно, желательно сдавать его в той же лаборатории, приблизительно в то же время. Откуда берут анализы на гормоны? Ответ на данный вопрос – из вены пациента. Срок готовности анализов зависит от конкретной лаборатории.






