Связи между людьми: виды и их особенности. ментальная связь
Содержание:
- Теория Бутлерова
- Простые и сложные
- Энергетическая связь
- Как образуется ионная и металлическая связь, примеры
- Подчинение и его способы
- Водородная связь
- Как обнаружить эмоциональную связь?
- Виды, особенности образования, как происходит, схема
- Основные виды словосочетаний
- Основные понятия
- Основные понятия
- Ключевая информация
- Слова и словосочетания
- Проверьте себя
- Виды связи между главным и зависимым словом в словосочетании
- Свойства связей
- Подчинительная связь в словосочетании: виды и их особенности
- Ионная связь
- Правило Октета
- H. + .H = H:H
- Способы образования
- Смысловая и грамматическая связь
- Ионная связь
Теория Бутлерова
Более успешная попытка объяснить природу химической связи веществ была предпринята русским ученым А.М.Бутлеровым. В основу своей теории этот ученый положил такие предположения:
- Атомы в соединенном состоянии связаны друг с другом в определенном порядке. Изменение этого порядка служит причиной образования нового вещества.
- Атомы связываются между собой по законам валентности.
- Свойства вещества зависят от порядка соединения атомов в молекуле вещества. Иной порядок расположения становится причиной изменения химических свойств вещества.
- Атомы, связанные между собой, наиболее сильно влияют друг на друга.
Теория Бутлерова объясняла свойства химических веществ не только их составом, но и порядком расположения атомов. Такой внутренний порядок А.М. Бутлеров назвал «химическим строением».
Теория русского ученого позволила навести порядок в классификации веществ и предоставила возможность определять строение молекул по их химическим свойствам. Также теория дала ответ на вопрос: почему молекулы, содержащие одинаковое количество атомов, имеют разные химические свойства.
Простые и сложные
Все словосочетания состоят из главной и зависимой частей. Например, в словосочетании чистая вода главная часть — вода, зависимая — чистая.
По своему составу словосочетания могут быть простыми и сложными. Простое словосочетание — это словосочетание, состоящее из двух знаменательных слов:
мокрые пятна, всегда весёлый, гулять в саду.
Сложное словосочетание — это словосочетание, состоящее из трёх и более знаменательных слов:
гулять в зимнем саду, стол из красного дерева.
Сложное словосочетание образуется путём распространения компонентов простого словосочетания и, следовательно, может быть разделено на простые:
папин стол из красного дерева – папин стол, стол из дерева, из красного дерева.
Энергетическая связь
Этот тип отношений обычно получает массу критики, поскольку далеко не все готовы углубляться в изучение каких-то энергетических каналов и привязок. Тем не менее становится все сложнее отрицать, что энергетическая связь между людьми существует. Как ее определить?

Возможно, вы хотя бы раз слышали, как человек говорит о своей сильной привязанности к другому. Специалисты в этой сфере настаивают на том, что именно подобная связь устанавливается за счет тонких энергетических трубочек, которые соединяют чакры людей. По таким каналам обычно начинает идти информация и налаживается общение.
Также стоит вспомнить выражение «сердечный человек». Но ведь для кого-то он может и не быть таковым. Все дело в том, что трубочки как раз и исходят из сердечной чакры. Поэтому, когда вы находите своего близкого человека, налаживается энергетическая связь.
Как образуется ионная и металлическая связь, примеры
Ионная связь образуется между металлом и неметаллом (иногда неметаллом и неметаллом) с разным уровнем электроотрицательности. Ионы могут быть простыми и иметь только один атом, как, например, Cl-, Na+, так и сложными и иметь несколько атомов и общий уровень заряда при них, как, например, NH4-.
Графически образование ионной связи можно проследить на схеме образования соединения натрия и хлора:
Металлическая связь образуется между двумя неметаллами. В связь вступают ионы металла и свободные электроны. Основой для образования металлической химической связи является наличие свободных атомных орбиталей, а также свободных электронов.
Схему образования металлической связи одной формулой можно записать следующим образом:
Число n будет зависеть от места химического элемента в Периодической системе химических элементов Д. И. Менделеева. Число внешних электронов равно номеру группы, в которой находится металл.
Подчинение и его способы
Смысловое соединение есть во всех конструкциях, а грамматическое – нет. Основные виды словосочетаний определяют по форме его составных элементов. Смотрим, изменяемые это части речи или нет, какой вид они имеют, какие средства связи слов в конструкции. Чтобы быстро определять тип соединения, нужно уметь изменять словоформы по падежам и лицам.
Существует 3 типа грамматической связи слов в минимальных синтаксических единицах. Рассмотрим подробно каждый из них.
Согласование
Способ сочетания, при котором зависимое слово принимает форму главного: шляпа (какая?) красивая. Оба члена имеют одинаковые падеж, род, число.
Согласование Внимание! Изменяется основной компонент – изменяется и второстепенный: шляпой красивой, шляпами красивыми, о шляпах красивых. Оба элемента в таких конструкциях – изменяемые части речи
Поэтому средства связи слов в сочетаниях такого типа – смысл и грамматический вид
Оба элемента в таких конструкциях – изменяемые части речи. Поэтому средства связи слов в сочетаниях такого типа – смысл и грамматический вид.
| Главное | Зависимое | Примеры |
| Существительное и те словоформы, которые могут выполнять его функцию | Прилагательное | Что-то (какое?) красивое,
небо (какое?) голубое, столовая (какая?) чистая |
| Причастие | Ученик (какой?) читающий,
река (какая?) замерзшая |
|
| Числительное | Дом (который?) второй,
в городах (скольких?) трех, руками (сколькими?) обеими |
|
| Местоимение | Человек (какой?) какой-то,
смысла (какого?) никакого, тарелка (чья?) моя |
|
| Существительное (приложение) | Девочка (какая?) Оля,
глаза (какие?) бусинки (глаза-бусинки) |
Управление
Главное слово управляет зависимым, ставит его в необходимую форму: пришел (с кем?) с другом – глагол указывает существительному на форму Т.п. Если изменить словоформу ведущего элемента, ведомый останется в том же падеже. Например: приду с другом, пришли с другом, придет с другом.
 Управление
Управление
Грамматические средства в этих конструкциях – смысл и падежная форма. Только при управлении между частями может ставиться предлог: думать о звездах, накричать на соседа, лететь навстречу ветру.
При управлении второстепенные слова – изменяемые части речи, так как соединяются с помощью падежных окончаний и/или предлогов.
| Главное | Зависимое | Примеры |
| Глагол,
деепричастие, существительное, причастие, прилагательное, числительное, местоимение. |
Существительное | Приехать (к кому?) к другу,
записывая (что?) лекцию, прочитана (кем?) мальчиком, память (о чем?) о прошлом, три (кого?) сестры, не нужен (кому?) никому. |
| Местоимение | Спросил (у кого?) у кого-то,
увидел (что?) нечто, подарок (кому?) ему |
|
| Прилагательное, называющее предмет | Узнать (о ком?) о неизвестном,
принесли (что?) горячее |
|
| Причастие, называющее предмет | Множество (кого?) собравшихся,
приветствовать (кого?) отдыхающих |
Необходимо различать! Числительное в именительном и винительном падежах командует существительным. Это управление: пять собак, трое мальчиков. Если числительное стоит в других падежах, то это согласование: пятью собаками, о пяти собаках, с тремя мальчиками, о трех мальчиках.
Примыкание
К главному компоненту примыкает неизменяемая часть речи: ехать (куда?) вперед. Средство соединения здесь одно – смысл, потому что ведомое слово не может принять иной вид. Можно выделить дополнительные средства соединения в таких конструкциях – порядок слов и интонацию.
 Примыкание
Примыкание
Зависимые компоненты в примыкании – неизменяемые, поэтому средство грамматической связи отсутствует. Ведущее слово – любая часть речи.
| Главное | Зависимое | Примеры |
| Глагол,
существительное, наречие, прилагательное, причастие, деепричастие, местоимение |
Наречие | Приехал (когда?) вчера,
дом (какой?) напротив, быстро (в какой степени?) очень |
| Деепричастие | Говорил (каким образом?) заикаясь | |
| Инфинитив | Мечта (какая?) жениться,
пришел (с какой целью?) поговорить |
|
| Неизменяемое имя прилагательное | Цвет (какой?) хаки | |
| Сравнительная степень имени прилагательного | Новость (какая?) поважнее,
некто (какой?) поинтереснее |
|
| Притяжательными местоимениями (его, ее, их) | Квартира (чья?) его,
ребенок (чей?) их |
|
| Существительное (несогласованное приложение) | Пьеса (какая?) «Бесприданница»,
роман (какой?) «Война и мир» |
Это интересно: Газопровод
Водородная связь
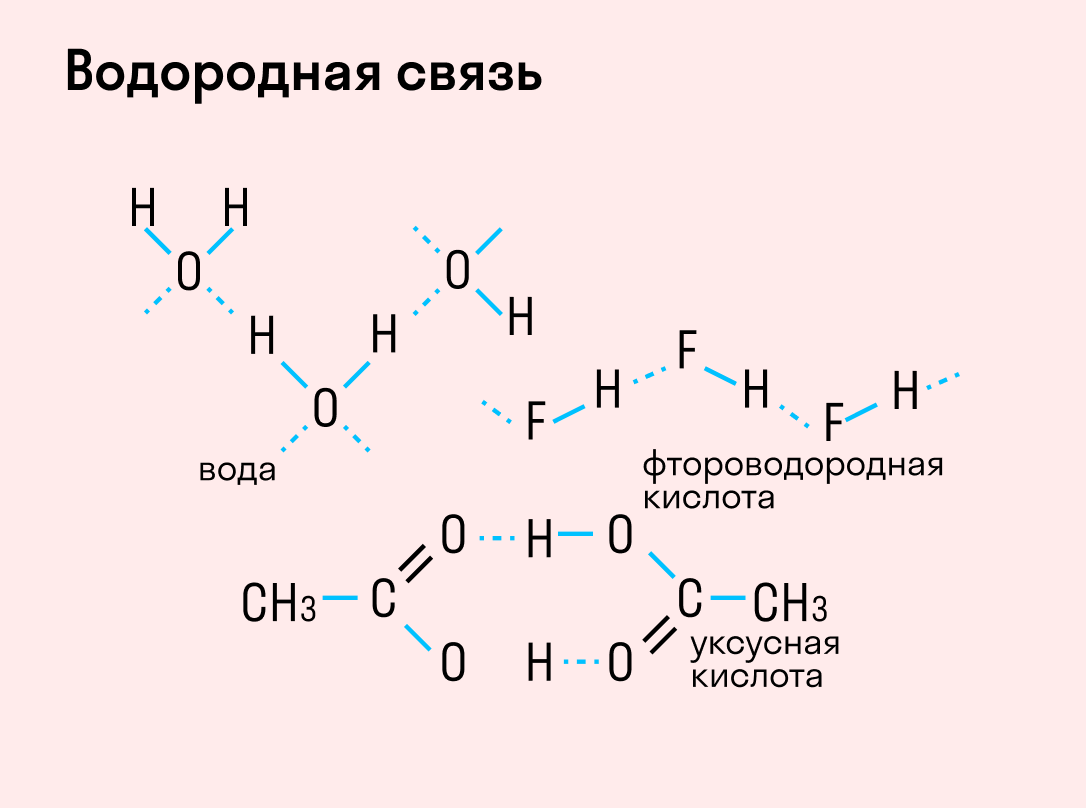
Данный тип связи в химии стоит отдельно, поскольку он может быть как внутри молекулы, так и между молекулами. Как правило, у неорганических веществ эта связь происходит между молекулами.
| Водородная связь образуется между молекулами, содержащими водород. Точнее, между атомами водорода в этих молекулах и атомами с большей ЭО в других молекулах вещества. |
Объясним подробнее механизм этого вида химической связи. Есть молекулы А и В, содержащие водород. При этом в молекуле А есть электроотрицательные атомы, а в молекуле В водород имеет ковалентную полярную связь с другими электроотрицательными атомами. В этом случае между атомом водорода в молекуле В и электроотрицательным атомом в молекуле А образуется водородная связь.
Такое взаимодействие носит донорно-акцепторный характер. Донором электронов в данном случае выступают электроотрицательные элементы, а акцептором — водород.
Графически водородная связь обозначается тремя точками. Ниже приведена схема такого взаимодействия на примере молекул воды.
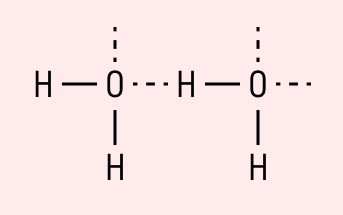
Важно!
В отдельных случаях водородная связь может образоваться внутри молекулы. Это характерно для органических веществ: многоатомных спиртов, углеводов, белковых соединений и т
д.
Характеристики водородной связи:
-
насыщенная,
-
направленная.
Как обнаружить эмоциональную связь?
Эмоциональные связи между людьми важны. Как их можно заметить? Присмотритесь, как ваш партнер реагирует на ваши эмоции. Если он понимает и правильно интерпретирует их, значит, у вас есть та самая связь.
Также таким людям всегда легко обсуждать самые острые темы, которые в других случаях могут вызывать ужасный дискомфорт. Если происходят спорные моменты, то каждый готов выслушать другого, а также спокойно высказать свою точку зрения.

Эмоциональная связь помогает восхищаться интеллектом партнера, увлекаться его личностью и легко общаться
Очень важно слушать и слышать друг друга, а также находить в глазах человека понимание ваших проблем
Вообще развивать эмоциональную связь очень полезно, особенно если речь идет об отношениях мужчины и женщины. Вряд ли подобное вам понадобится в общении с коллегами или конкурентами, там-то как раз нужен холодный расчет. Но иметь человека, с которым вы сможете проявлять эмоции, хочет каждый.
Если вы налаживаете эту связь, вы перестаете замечать внешность человека, оценивая его внутреннюю красоту. Легко говорите на важные темы и понимаете совершенно иное мышление. Проблемы решать становится в разы легче, а коммуникация только растет. В хорошо развитых эмоциональных отношениях вы чувствуете себя частью чего-то огромного, светлого и настоящего.
Виды, особенности образования, как происходит, схема
Металлическая связь не может существовать между отдельными соединенными между собой атомами. Она появляется только в веществах.
При этом связи в этих веществах не отличаются постоянством. Электроны, отделившиеся от атомов металлов, превращаются в «электронный газ», благодаря чему они могут спокойно путешествовать по кристаллической решетке.
Основой для образования металлической химической связи является наличие свободных атомных орбиталей, а также свободных электронов.
Схему образования металлической связи можно записать следующим образом:
Число n будет зависеть от места химического элемента в Периодической системе химических элементов Д. И. Менделеева. Число внешних электронов равно номеру группы, в которой находится металл.
Характерные кристаллические решетки
Кристаллическая решетка в веществах с металлической связью является основой, неким каркасом кристалла, в узлах которой находятся ионы металла, а между ними в виде «электронного газа» перемещаются отрицательно заряженные электроны, периодически присоединяющиеся к ионам металлов, превращая их в атомы.
Форма кристаллической решетки отличается в зависимости от группы, к которой относится металл:
- щелочные металлы (литий Li, калий K, рубидий Rb и другие) имеют объемно-центрированную кубическую кристаллическую решетку;
- переходные элементы (алюминий Al, медь Cu, цинк Zn и другие) имеют гранецентрированную кубическую форму решетки;
- щелочноземельные металлы (бериллий Be, кальций Ca, радий Ra, кроме бария) имеют гексагональную решетку;
- индий In имеет тетрагональную решетку;
- ртуть Hg имеет ромбоэдрическую решетку.
Ромбоэдрическая решетка
Основные виды словосочетаний
По количеству компонентов словосочетания бывают простыми и сложными.
Простые словосочетания — это конструкция из одного главного и одного зависимого компонента: разговор о жизни, сидеть на стуле.
Сложными называют словосочетания, которые состоят из трех и более компонентов. Сложные словосочетания бывают трех типов:
-
словосочетания с последовательным подчинением: очень быстро бежать;
-
словосочетания с параллельным подчинением: знаменитое произведение поэта;
-
комбинированные словосочетания с последовательным и параллельным подчинением: провести вечер с хорошими друзьями.
Существует три вида связи между словами в словосочетании:
-
согласование — вид связи, при котором зависимое слово равняется в своей форме главному слову, то есть согласуется с ним в роде, числе и падеже: необычный прибор, об интересном событии;
-
управление — вид связи, при котором зависимое слово употребляется в определенной падежной форме в зависимости от лексико-грамматического значения главного слова: симпатия к соседу, слушать лекцию;
-
примыкание — вид связи, при котором зависимость слова выражается лексически, порядком слов и интонацией, без применения служебных слов или морфологического изменения: петь звонко, смотреть молча.
По степени слитности компонентов выделяют словосочетания:
-
синтаксически свободные: высокий дом, идти в школу;
-
синтаксически или фразеологически несвободные, которые образуют синтаксическое единство и выступают в предложении в роли одного члена: три сестры, анютины глазки, бить челом.
Смысловые отношения можно определить при помощи вопросов:
-
Чей?, Какой?, Который? — определительные.
Пиджак (чей?) папы; красное (какое?) платье.
-
Кого?, Чего? — объектные.
Подарок (кому?) подруге.
-
Куда?, Как?, Когда? — обстоятельственные.
Гулять (где?) в парке.
Основная классификация словосочетаний основана на морфологических свойствах главного слова. В зависимости от того, какой частью речи оно выражено, выделяют три группы подчинительных словосочетаний: именные, глагольные, наречные.
Основные понятия
- Словосочетание — это сочетание самостоятельных слов, связанных по смыслу и грамматически.
- Подчинительная связь — это способ связи слов в словосочетании, когда одно слово главное, а другое — зависимое. От главного к зависимому всегда можно поставить вопрос.
Словосочетание состоит из главного и зависимого слова.
Например: Сергей вовремя сдал свою работу. Найдем все словосочетания:
- сдал работу – сдал (кого? что?) работу; сдал – главное слово, работу – зависимое;
- вовремя сдал – сдал (когда?) вовремя; сдал – главное слово, вовремя – зависимое;
- свою работу – работу (какую? чью?) свою; работу – главное слово, свою – зависимое.
Остались два слова: Сергей сдал. Это грамматическая основа, оба слова — главные члены предложения, ни одно из них не является главнее другого. Получается, что подлежащее и сказуемое нельзя назвать словосочетанием.
Основные понятия
- Словосочетание — это сочетание самостоятельных слов, связанных по смыслу и грамматически.
- Подчинительная связь — это способ связи слов в словосочетании, когда одно слово главное, а другое — зависимое. От главного к зависимому всегда можно поставить вопрос.
Словосочетание состоит из главного и зависимого слова.
Например: Сергей вовремя сдал свою работу. Найдем все словосочетания:
- сдал работу – сдал (кого? что?) работу; сдал – главное слово, работу – зависимое;
- вовремя сдал – сдал (когда?) вовремя; сдал – главное слово, вовремя – зависимое;
- свою работу – работу (какую? чью?) свою; работу – главное слово, свою – зависимое.
Остались два слова: Сергей сдал. Это грамматическая основа, оба слова — главные члены предложения, ни одно из них не является главнее другого. Получается, что подлежащее и сказуемое нельзя назвать словосочетанием.
Ключевая информация
В химической науке существует четыре основных типа связи — ковалентная, ионная, металлическая и водородная. Металлическая возникает между элементами-металлами, водородная — между молекулами, состоящими из водорода и атомов с высокой электроотрицательностью (азотом, кислородом, фтором).
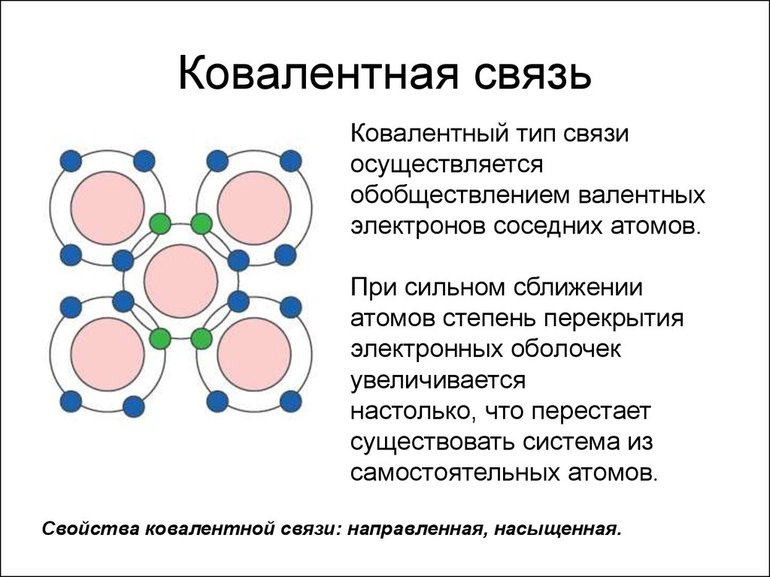
Самые разнообразные соединения относятся к ковалентной и ионной связям, которые представляют по своему составу смешанный тип. Для ионной связи ковалентная в определенном смысле выполняет материнскую функцию.
Наиболее частым и распространенным видом химической связи считается именно ковалентная. Это соединение, в процессе формирования которого обобществляется (перекрывается) пара валентных электронных облаков. Количество таких связей, образованных атомом элемента, — это показатель ковалентности.
Ковалентная связь бывает двух типов — неполярная и полярная. Определяющими факторами для типа связи служат значения электроотрицательности взаимодействующих атомов химических элементов. Если эти показатели у атомов:
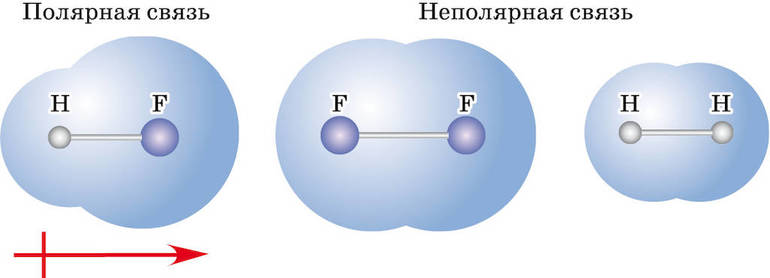
- равны или примерно равны (разница между значениями по шкале Полинга — до 0,4) — это ковалентная неполярная связь (общая электронная пара не смещается ни к одному из атомов);
- отличаются, но не сильно (разница от 0,4 до 1,7) — это ковалентная полярная связь (электронная пара смещается к одному из участвующих атомов);
- отличаются сильно (разница более 1,7) — это ионная связь (один или несколько электронов не просто смещаются, а почти полностью переходят к другому атому, причем всегда к тому, у которого значение электроотрицательности больше, при этом оба атома-участника превращаются в ионы).
Электростатическое притяжение частиц в ионной связи очень сильное. Эта особенность обусловливает высокие температуры плавления и кипения для веществ с такой связью. Однако стопроцентного ионного соединения не существует. Электронная пара не переходит к более электроотрицательному атому полностью. В качестве яркого примера наиболее сильного смещения электронов стоит привести фторид цезия CsF. Так называемая «степень ионности» в этом соединении достигает 97%.
Слова и словосочетания
В синтаксисе русского языка наименьшей значимой единицей является слово. А слово имеет способность объединяться с другим словом и образовать словосочетание, которое находится на следующем уровне синтаксиса.
Слова и словосочетания, объединяясь по смыслу и грамматически, создают сообщение, оформленное в виде предложения. Это можно представить в виде лесенки, на первой ступеньке которой находится отдельное слово, или лексема, на второй ступеньке — словосочетание как более сложная синтаксическая единица, а на третьей — предложение и сложные синтаксические конструкции, состоящие из нескольких предложений, соединенных бессоюзной, и связью.

Проверьте себя
Определите, к какому виду сложного предложения относятся эти примеры: сложноподчиненному или сложносочиненному?
-
Мать уже наготовила на утро и легла спать, когда я вернулся из театра.
-
Я знал: это не может продолжаться слишком долго.
-
Снежинки легким пухом ложились на ладонь, и мир вокруг застыл в белоснежном великолепии.
-
Я вышел на опушку леса спустя час, но путешественников и след простыл.
-
Я быстро нашел место, где гнездились кукушки.
Курсы подготовки к ЕГЭ по русскому языку в онлайн-школе Skysmart — без стресса и на реальных экзаменационных заданиях. Попробуйте бесплатно на вводном уроке!
Виды связи между главным и зависимым словом в словосочетании
Они определяются по характеру зависимости. Так, если зависимое слово полностью подстраивается под главное по грамматическим признакам, это согласование. С грамматической точки зрения главное слово является ведущим, это правило главного слова в словосочетании. Для того, чтобы понять характер такой грамматической связи, нужно разобрать правильное и неправильное словосочетания:
- рабочее место – в нем главным словом является существительное третьего лица в единственном числе, зависимое слово – прилагательное – также ставится в эту формы;
- рабочее места – главным словом снова является существительное третьего лица, но во множественном числе, прилагательное же стоит в единственном, значит, в словосочетании допущена грамматическая ошибка.
Это самая простая пара, так как главное слово в ней всегда существительное, а зависимым обычно является прилагательное, но также на этом месте может быть числительное или причастие.
Второй вид связи – управление. При этом к главному слову “подставляется” зависимое, которое всегда идет в форме косвенного падежа, при этом предлог может добавляться или нет. Грамматическое изменение главного слова не влечет за собой изменение зависимого. В качестве главного слова могут выступать разные части речи: подстилка кота, гулять с котом.
Наконец, примыкание – это сугубо смысловая связь без грамматической зависимости. В качестве главного слова в нем также могут выступать разные части речи: долго спать, знать ее.
Свойства связей
Чтобы провести сравнение разных химических реакций используются разные количественные характеристики, такие как:
- длина,
- энергия,
- полярность,
- порядок связей.
Разберем их подробнее.
Длина связи – равновесное расстояние между ядрами атомов, которые соединены химической связью. Обычно измеряется экспериментально.
Энергия химической связи определяет ее прочность. В данном случае под энергией подразумевается усилие, необходимое, для того, чтобы разорвать химическую связь и разъединить атомы.
Полярность химической связи показывает, насколько электронная плотность смещена к одному из атомов. Способность атомов смещать к себе электронную плотность или говоря простым языком «тянуть одеяло на себя» в химии называют электроотрицательностью.
Порядок химической связи (другими словами кратность химической связи) – это число электронных пар, вступающих в химическую связь. Порядок может быть, как целым, так и дробным, чем он выше, тем большее число электронов осуществляют химическую связь и тем труднее ее разорвать.
Подчинительная связь в словосочетании: виды и их особенности
Разобраться в особенностях подчинения поможет таблица:
|
Название вида связи |
Главное слово |
Зависимое слово |
Признаки |
|
Согласование |
Существительное |
Прилагательное, числительное |
Зависимое слово принимает грамматическую форму главного, когда оно изменяется – изменяется и зависимое |
|
Управление |
Глагол, существительное |
Существительное, местоимение |
Главное слово может изменяться, зависимое вместе с ним не изменяется (стоит всегда в определённом косвенном падеже) |
|
Примыкание |
Глагол, наречие, прилагательное |
Наречие, глагол в начальной форме |
Слова связаны только значением, без грамматической связи |
Все три вида связи в словосочетании предполагают, что вопросы задаются от главного слова к зависимому. Это дополнительный метод определения того, какая связь использована. Чтобы было понятнее, стоит рассмотреть разобранные примеры.
Ионная связь
Ионная химическая связь является пограничной ковалентной полярной. Отличаются тем, что для веществ, в которых локализуется ковалентная связь, характерно существование совместной электронной пары, тогда как для ионной связи свойственна полная отдача электронов. Следствием отдачи является образование заряженных частиц – ионов.

Определить тип связи помогут вычисления. Если разность значений электроотрицательностей больше 1,7, то для вещества характерна ионная связь. Если значение меньше 1,7, то свойственная полярная связь. Рассмотрим два вещества NaCl и СаС2. Оба они образованы металлом (Na и Са) и неметаллом (Clи С). Однако в одном случае связь будет ионная, во втором – ковалентная полярная.

Постулат физики гласит, что противоположности притягиваются. Т.е. положительные ионы притягивают отрицательные и наоборот.

Допустим, что необходимо получить вещество с атомов калия и фтора. Каждый атом стремится заполучить конфигурацию благородного газа. Достигнуть этого возможно двумя способами отдав или приняв электроны, образуя при этом ионы с желаемой конфигурацией.
Атому калия гораздо проще отдать 1 электрон, чем забрать у фтора 7. Принимая 1 электрон, F имеет завершённый уровень.

Аналогично калий, который с лёгкостью отдал свой электрон, его катион принял электронную формулу аргона.
Кальций двухвалентный металл, то для взаимодействия необходимо два атома фтора, поскольку он способен принять только один электрон. Схема образования ионной связи имеет вид.

Данный вид связи локализуется во всех солях, между металлом и кислотным остатком. В выше приведённом примере для угольной кислоты, кислотным остатком будет СО32−, если вместо водорода поставить атомы натрия, то схема образования связи имеет вид.

Следует отметить, что ионная связь будет существовать между Naи О, а между С и О ковалентная полярная.
Правило Октета
Электронная конфигурация атома особенно стабильна (иными словами, имеет минимальный запас энергии, что всегда предпочтительно), когда внешняя электронная оболочка заполнена. Поэтому атомы склонны к таким превращениям, в результате которых во внешнем слое оказывается „магическое” число электронов — восемь. Исключение составляют атомы первых двух элементов периодической системы, для которых предпочтительно образование двухэлектронной внешней оболочки.
Модели атомов инертных газов
Правило октета объясняет, почему инертные газы (группа VIIIA) гелий, неон и аргон обычно не вступают в химические реакции. Их внешняя электронная оболочка уже заполнена, следовательно нет необходимости во взаимодействии с другими атомами с целью принять, отдать или объединить электроны.
Элементы 3—7-го периодов также обычно подчиняются правилу октета (т. е. склонны к заполнению s- и р-орбиталей, хотя могут иметься d- и f-орбитали).
Согласно правилу октета большинство атомов склонно принимать, отдавать или объединять электроны с тем, чтобы создать восьмиэлектронную внешнюю оболочку.
H. + .H = H:H
Таким образом, в молекуле водорода одна общая электронная пара и одна химическая связь H–H. Эта электронная пара не смещается ни к одному из атомов водорода, т.к. электроотрицательность у атомов водорода одинаковая. Такая связь называется ковалентной неполярной.
Ковалентная неполярная (симметричная) связь – это ковалентная связь, образованная атомами с равной элетроотрицательностью (как правило, одинаковыми неметаллами) и, следовательно, с равномерным распределением электронной плотности между ядрами атомов.
Дипольный момент неполярных связей равен 0.
Примеры: H2 (H-H), O2 (O=O), S8.
Ковалентная полярная химическая связь
Ковалентная полярная связь – это ковалентная связь, которая возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией).
Электронная плотность смещена к более электроотрицательному атому – следовательно, на нем возникает частичный отрицательный заряд (δ-), а на менее электроотрицательном атоме возникает частичный положительный заряд (δ+, дельта +).
Чем больше различие в электроотрицательностях атомов, тем выше полярность связи и тем больше дипольный момент. Между соседними молекулами и противоположными по знаку зарядами действуют дополнительные силы притяжения, что увеличивает прочность связи.
Полярность связи влияет на физические и химические свойства соединений. От полярности связи зависят механизмы реакций и даже реакционная способность соседних связей. Полярность связи зачастую определяет полярность молекулы и, таким образом, непосредственно влияет на такие физические свойства как температуре кипения и температура плавления, растворимость в полярных растворителях.
Примеры: HCl, CO2, NH3.
Механизмы образования ковалентной связи
Ковалентная химическая связь может возникать по 2 механизмам:
1. Обменный механизм образования ковалентной химической связи – это когда каждая частица предоставляет для образования общей электронной пары один неспаренный электрон:
Способы образования
Слова объединяются подчинительным способом. Это значит, что они неравноправны: одно – главное, другое – зависимое. Функция такого соединения – более подробно описать понятие (предмет, признак, действие).
Виды словосочетаний Важно! Не каждое сочетание слов может стать словосочетанием. Какие разновидности словесных сочетаний не относятся к словосочетаниям:
Какие разновидности словесных сочетаний не относятся к словосочетаниям:
- Грамматическая основа – подлежащее и сказуемое: папа приехал, окно открыто, задача решена.
- Однородные члены предложения. Они связаны сочинительными союзами: добрый и веселый, то грустно, то смешно, не только умный, но и красивый.
- Сложное будущее время: буду читать, будем смеяться.
- Сравнительная степень: самый быстрый, менее высоко.
- Служебные части речи с самостоятельными: в течение времени, возле реки, навстречу ветру.
- Фразеологизмы. По смыслу они приравниваются к словам: вешать нос (расстраиваться), скрепя сердце (неохотно).
Слова в словосочетании соединяются:
- по смыслу (от главного элемента задается смысловой вопрос: написать (что?) книгу, зайти (куда?) домой),
- грамматически: с помощью окончаний: курткой желтой, либо с помощью окончаний и предлогов: зацепиться за ветку.
Чтобы лучше понять, что такое зависимое слово, посмотрим, какие встречаются смысловые отношения:
- Определительные. Называется признак предмета: фрукты (какие?) вкусные.
- Объектные. Указывается на объект действия, место, направление: приехать (к кому?) к другу, повернуть (куда?) направо.
- Обстоятельственные. Обозначается признак действия: бежать (каким образом?) быстро.
Смысловая и грамматическая связь
Смысловая связь слов в словосочетаниях устанавливается по вопросам, которые задаются от главного слова к зависимому:
| Смысловая связь | Примеры |
|---|---|
| предмет и его признак |
засохший цветок цветок (какой?) засохший |
| действие и предмет |
лететь к солнцу лететь (к чему?) к солнцу |
| действие и его признак |
заинтересованно разглядывать разглядывать (как?) заинтересованно |
| признак и его степень |
по-весеннему свежий свежий (как?) по-весеннему |
Зависимое слово связывается с главным не только по смыслу, но и грамматически. Грамматическая связь слов в словосочетании чаще всего выражается с помощью окончания или с помощью окончания и предлога:
домашние тапочки, тапочки (какие?) домашние;
ходить по лезвию, ходить (по чему?) по лезвию.
Ионная связь
Образование ионной химической связи возникает при взаимном электрическом притяжении двух ионов, имеющих разные заряды. Ионы обычно при таких химических связях простые, состоящие из одного атома вещества.
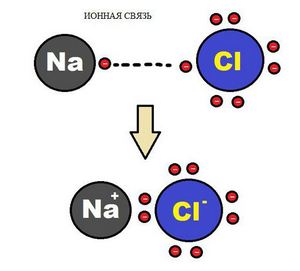
Схема ионной химической связи.
Характерной особенностью ионного типа химичечкой связи является отсутствие у нее насыщенности, и как результат, к иону или даже целой группе ионов может присоединиться самое разное количество противоположно заряженных ионов. Примером ионной химической связи может служить соединение фторида цезия CsF, в котором уровень «ионости» составляет практически 97%.






