Атф-синтаза
Содержание:
- Как образуется АТФ в организме?
- Структура и функции АТФ
- Синтез молекулы АТФ
- Строение АТФ и биологическая роль молекулы. Дополнительные функции аденозинтрифосфата
- Достоинства и недостатки
- Световая фаза фотосинтеза
- Как отличить подделку
- Внешние ссылки [ править ]
- Функции АТФ
- Роль АТФ в энергетическом балансе
- Структура АТФ-синтазы
- Синтез АТФ в организме
- История создания ATF
- Окислительное фосфорилирование
Как образуется АТФ в организме?
Синтез аденозинтрифосфорной кислоты идёт постоянно, т. к. энергия организму для нормальной жизнедеятельности нужна всегда. В каждый конкретный момент содержится совсем немного этого вещества — примерно 250 граммов, которые являются «неприкосновенным запасом» на «чёрный день». Во время болезни идёт интенсивный синтез этой кислоты, потому что требуется много энергии для работы иммунной и выделительной систем, а также системы терморегуляции организма, что необходимо для эффективной борьбы с начавшимся недугом.
В каких клетках АТФ больше всего? Это клетки мышечной и нервной тканей, поскольку в них наиболее интенсивно идут процессы энергообмена. И это очевидно, ведь мышцы участвуют в движении, требующем сокращения мышечных волокон, а нейроны передают электрические импульсы, без которых невозможна работа всех систем организма
Поэтому так важно для клетки поддерживать неизменный и высокий уровень аденозинтрифосфата
Каким же образом в организме могут образовываться молекулы аденозинтрифосфата? Они образуются путём так называемого фосфорилирования АДФ (аденозиндифосфата). Эта химическая реакция выглядит следующим образом:
АДФ + фосфорная кислота + энергия→АТФ + вода.
Фосфорилирование же АДФ происходит при участии таких катализаторов, как ферменты и свет, и осуществляется одним из трёх способов:
- фотофосфорилирование (фотосинтез у растений) ;
- окислительное фосфорилирование АДФ Н-зависимой АТФ-синтáзой, в результате которого основная масса аденозинтрифосфата образуется на мембранах митохондрий клеток (связано с дыханием клетки);
- субстратное фосфорилирование в цитоплазме клетки в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений, не требующее участия мембранных ферментов.
Как окислительное, так и субстратное фосфорилирование использует энергию веществ, окисляющихся в процессе такого синтеза.
Структура и функции АТФ
Как вы помните, нуклеиновые кислотысостоят из нуклеотидов. Оказалось, что в клетке нуклеотиды могут находиться в связанном состоянии или в свободном состоянии. В свободном состоянии они выполняют ряд важных для жизнедеятельности организма функций.
К таким свободным нуклеотидам относится молекула АТФ или аденозинтрифосфорная кислота (аденозинтрифосфат). Как и все нуклеотиды, АТФ состоит из пятиуглеродного сахара – рибозы, азотистого основания – аденина, и, в отличие от нуклеотидов ДНК и РНК, трех остатков фосфорной кислоты (рис. 1).


Рис. 1. Три схематических изображения АТФ
Важнейшая функция АТФ состоит в том, что она является универсальным хранителем и переносчиком энергии в клетке.
Все биохимические реакции в клетке, которые требуют затрат энергии, в качестве ее источника используют АТФ.
При отделении одного остатка фосфорной кислоты, АТФ переходит в АДФ (аденозиндифосфат). Если отделяется ещё один остаток фосфорной кислоты (что случается в особых случаях), АДФ переходит в АМФ (аденозинмонофосфат) (рис. 2).

Рис. 2. Гидролиза АТФ и превращение её в АДФ
При отделении второго и третьего остатков фосфорной кислоты освобождается большое количество энергии, до 40 кДж. Именно поэтому связь между этими остатками фосфорной кислоты называют макроэргической и обозначают соответственным символом.
При гидролизе обычной связи выделяется (или поглощается) небольшое количество энергии, а при гидролизе макроэргической связи выделяется намного больше энергии (40 кДж). Связь между рибозой и первым остатком фосфорной кислоты не является макроэргической, при её гидролизе выделяется всего 14 кДж энергии.
Макроэргические соединения могут образовываться и на основе других нуклеотидов, например ГТФ (гуанозинтрифосфат) используется как источник энергии в биосинтезе белка, принимает участие в реакциях передачи сигнала, является субстратом для синтеза РНК в процессе транскрипции, но именно АТФ является наиболее распространенным и универсальным источником энергии в клетке.
АТФ содержится как в цитоплазме, так и в ядре, митохондриях и хлоропластах.
Таким образом, мы вспомнили, что такое АТФ, каковы её функции, и что такое макроэргическая связь.
Синтез молекулы АТФ
27 декабря, 2010
Существуют две гипотезы, объясняющие механизм синтеза АТФ — прямой и косвенный. Согласно прямому механизму, АДФ и Фн (неорганический фосфат) связываются с активным центром фермента, куда по каналу поступают протоны. Протоны взаимодействуют с кислородом Фн с образованием воды. Это делает Фн активным, и он присоединяется к АДФ. После этого молекула АТФ отделяется от фермента.
Согласно второй гипотезе, синтез АТФ из АДФ и Фн происходит в активном центре фермента самопроизвольно. Однако образующаяся при этом молекула АТФ прочно связывается с ферментом, поэтому для ее освобождения затрачивается энергия протонного градиента. Предполагают, что структурные перестройки фермента, приводящие к высвобождению АТФ, связаны с циклическими процессами протонирования и депротонирования функционально важных групп фермента. Что сейчас все больше находит экспериментальные подтверждения. Доказательством того, что именно градиент протона обеспечивает фосфорилирование, являются опыты с разобщителями окисления и фосфорилирования. Наиболее часто, в качестве разобщителя, выступает динитрофенол, он делает мембрану проницаемой для протонов и тем самым ликвидирует протонный градиент. При этом скорость окисления даже усиливается, однако образование АТФ не происходит. Таким образом, процесс окисления сопряжен с процессом фосфорилирования. Степень сопряженности окисления и фосфорилирования может быть разной в зависимости от условий и от состояния клеток. Показателем сопряженности окисления и фосфорилирования служит коэффициент фосфорилирования Р/О, который соответствует отношению количества связанного неорганического фосфора (АДФ + Фн —> АТФ) к поглощенному в процессе дыхания кислороду. Как уже рассматривалось выше, перенос двух электронов к кислороду по дыхательной цепи сопровождается не более чем тремя фосфорилированиями. Следовательно, коэффициент Р/О может быть не более 3. На величину Р/О оказывают влияние внешние условия. При засухе окисление усиливается, а накопление энергии в виде АТФ не происходит, коэффициент Р/О резко падает. Коэффициент фосфорилирования резко падает и при заболевании организмов. В ряде случаев может наблюдаться непосредственное использование энергии протонного градиента (∆μ Н+). Действительно, поскольку внутренняя сторона мембраны оказывается заряженной отрицательно, возникает трансмембранный потенциал. Катионы в силу электрического притяжения могут поступать и накапливаться во внутреннем пространстве митохондрий. Имеются данные, что протонный градиент может обеспечить также приток углеводов, в частности поступление сахарозы в ситовидные трубки. Таким образом, ∆μ Н+ обеспечивает осмотическую работу и транспорт веществ против градиента их концентрации. Наконец, показана возможность использования ∆μ Н+ на механическую работу (движение бактерий)
Вместе с тем важно отметить, что ∆μ Н+ может играть роль как транспортная форма энергии, передаваясь вдоль мембран (В.П. Скулачев)
Таким образом, клетка обладает двумя формами используемой энергии, двумя энергетическими «валютами» — АТФ и ∆μ Н+
1) АТФ — химическая «валюта», растворимая в воде и легко используемая в водной фазе; 2) ∆μ Н+ — электрохимическая, неразрывно связанная с мембранами.
Важно заметить, что эти две формы используемой клеткой энергии могут переходить друг в друга. При образовании АТФ используется энергия ∆μ Н+, при распаде АТФ энергия может аккумулироваться в ∆μ Н+
Биохимия, Физиология растенй
Строение АТФ и биологическая роль молекулы. Дополнительные функции аденозинтрифосфата
Кроме энергетической, АТФ может выполнять множество других функций в клетке. Наряду с другими нуклеотидтрифосфатами трифосфат участвует в построении нуклеиновый кислот. В этом случае АТФ, ГТФ, ТТФ, ЦТФ и УТФ являются поставщиками азотистых оснований. Это свойство используется в процессах и транскрипции.
Также АТФ необходим для работы ионных каналов. Например, Na-K канал выкачивает 3 молекулы натрия из клетки и вкачивает 2 молекулы калия в клетку. Такой ток ионов нужен для поддержания положительного заряда на наружной поверхности мембраны, и только с помощью аденозинтрифосфата канал может функционировать. То же касается протонных и кальциевых каналов.
АТФ является предшественником вторичного мессенжера цАМФ (циклический аденозинмонофосфат) — цАМФ не только передает сигнал, полученный рецепторами мембраны клетки, но и является аллостерическим эффектором. Аллостерические эффекторы — это вещества, которые ускоряют или замедляют ферментативные реакции. Так, циклический аденозинтрифосфат ингибирует синтез фермента, который катализирует расщепление лактозы в клетках бактерии.
Сама молекула аденозинтрифосфата также может быть аллостерическим эффектором. Причем в подобных процессах антагонистом АТФ выступает АДФ: если трифосфат ускоряет реакцию, то дифосфат затормаживает, и наоборот. Таковы функции и строение АТФ.

Достоинства и недостатки
Как и любой металл, материал, деталь или что-то другое, смазывающая жидкость ATF 2 от компании ЗИК имеет свои плюсы и минусы.
У смазки есть преимущества перед конкурентами:
- стабильно при термоокислительных процессах;
- хорошо совмещается с любым материалом уплотнителя;
- при любых температурах, особенно минусовых, передача переключается мягко, чётко и комфортно;
- трансмиссия работает бесшумно;
- имеются свойства — высокая антикоррозия;
- при использовании в низких температурах, текучесть на высоте;
- ресурс срока службы всех систем продлевается.
В том случае, если жидкость используется в соответствии со всеми регламентами и предписаниями недостатков у рассматриваемого трансмиссионного масла быть не может.
Световая фаза фотосинтеза
Чтобы лучше понять, что происходит во время фотосинтеза, разберём фазы фотосинтеза. Световая фаза фотосинтеза включает в себя фотохимические и фотофизические процессы, и может быть поделена на три этапа:
- Фаза поглощения — энергия света улавливается при помощи светособирающих комплексов, переходит в энергию электронного возбуждения пигментов, передаётся в реакционный центр фотосистем I и II.
- Фаза реакционных центров — энергия электронного возбуждения пигментов светособирающих комплексов используется для активации реакционных центров фотосистем. В реакционном центре электрон от возбуждённого хлорофилла передаётся другим компонентам электрон-транспортной цепи, пигмент после отдачи электрона переходит в окисленное состояние и становится способным, в свою очередь, отнимать электроны у других веществ. Именно в этом процессе происходит преобразование физической формы энергии в химическую.
- Фаза электрон-транспортной цепи — электроны переносятся по цепи переносчиков, образуются АТФ, НАДФН, O2. Необходимо, чтобы каждый переносчик электрон-транспортной цепи поочерёдно восстанавливался и окислялся, обеспечивая таким образом перенос энергии электронов. Любой этап переноса электрона сопровождается высвобождением или поглощением энергии. Часть энергии теряется. На некоторых участках электрон-транспортной цепи перенос электрона сопряжён с переносом протона.
Для того чтобы понять, что происходит во время фазы фотосинтеза, рассмотрим эти процессы подробнее. Кванты света улавливаются светособирающими комплексами фотосистемы I — молекула хлорофилла в составе светособирающего комплекса переходит в возбуждённое состояние, и энергия передаётся в реакционный центр фотосистемы I. Происходит возбуждение молекул хлорофилла фотосистемы I, отщепляется электрон. Пройдя по цепочке внутренних компонентов фотосистемы I и внешних переносчиков, электрон в конце концов попадает к НАДФ+ — образуется восстановитель НАДФН. Получается, что хлорофилл фотосистемы I отдал электрон и приобрёл положительный заряд, и для дальнейшего функционирования необходимо восстановить нейтральность молекулы, получить электрон, чтобы закрыть «дырку». Этот электрон приходит от фотосистемы II.
На светособирающие комплексы фотосистемы II попадают кванты света — происходит возбуждение молекулы хлорофилла фотосистемы II, молекула хлорофилла отдаёт электрон и переходит в окисленное состояние. Нехватку электрона хлорофилл восполняет благодаря фотолизу воды, при этом образуется протоны H+, а также важный побочный продукт фотосинтеза — кислород. По цепи переносчиков электрон от хлорофилла фотосистемы II попадает к хлорофиллу реакционного центра фотосистемы I и восстанавливает его. Теперь этот хлорофилл может снова поглощать энергию кванта света и отдавать электрон в электрон-транспортную цепь.
Протоны, попадающие во внутритилакоидное пространство, используются для синтеза АТФ. С помощью фермента АТФ-синтазы за счёт градиента протонов образуется АТФ из АДФ и фосфата. Под градиентом понимают неравномерное распределение: во внутритилакоидном пространстве H+ больше, в строме — меньше. Поэтому частицы стремятся проникнуть в строму, переходят в неё через АТФ-синтазу, а в процессе пути сквозь белковый комплекс отдают ему часть энергии, которая и используется для синтеза АТФ.
Как отличить подделку
Компания-производитель постоянно ведёт усовершенствование защиты своего продукта от фальшивок. Чтобы купить оригинал ZIC ATF Dexron 2 и не расстроится, что это не подделка, необходимо знать следующее:
- Канистра имеет полностью красный цвет и красные этикетки.
- Крышка упакована термопленкой с надписью SK.
- Сняв крышку сразу же видна ещё одна защита.
- Прозрачная мерная шкала.
- Вдоль вертикальной полосы голограмма.
- Этикетка тыльной стороны имеет выпуклый текст, который можно почувствовать пальцами.
- На дно канистр, компания ставит фирменный штамп.
- Упаковка выполненное из не из однородного пластика, а с разной фактурой.
Самое главное производить покупку горюче-смазочных материалов в официальных сетях и магазинах.
Внешние ссылки [ править ]
| vтеМембранный транспортный белок : ионные каналы ( TC 1A ) | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
| см. также расстройства |
Функции АТФ
Источник энергии
АТФ является основным носителем энергии, которая используется для всех клеточных активностей. Когда АТФ гидролизуется и превращается в аденозиндифосфат (АДФ), выделяется энергия. Удаление одной фосфатной группы высвобождает 7,3 килокалорий на моль или 30,6 кДж на моль при стандартных условиях. Эта энергия питает все реакции, которые происходят внутри клетки. АДФ также может быть преобразован обратно в АТФ, так что энергия доступна для других клеточных реакций.
АТФ производится несколькими различными способами. Фотофосфорилирование – это метод, специфичный для растений и цианобактерий. Это создание АТФ из АДФ с использованием энергии солнечного света, и происходит во время фотосинтез, АТФ также образуется из процесса клеточного дыхания в митохондрии клетки. Это может быть через аэробного дыхания, который требует кислорода, или анаэробное дыхание, чего нет. Аэробного дыхания производит АТФ (наряду с углекислым газом и водой) из глюкозы и кислорода. Анаэробное дыхание использует химические вещества, кроме кислорода, и этот процесс в основном используется археями и бактерии которые живут в анаэробных условиях. Ферментация является еще одним способом получения АТФ, который не требует кислорода; он отличается от анаэробного дыхания, потому что он не использует цепь переноса электронов, Дрожжи и бактерии являются примерами организмов, которые используют ферментацию для образования АТФ.
Передача сигнала
АТФ является сигнальной молекулой, используемой для клеточной коммуникации. Киназы, которые являются ферментами, которые фосфорилируют молекулы, используют АТФ в качестве источника фосфатных групп. Киназы важны для передачи сигнала, то есть как физический или химический сигнал передается от рецепторов снаружи клетки внутрь клетки. Как только сигнал находится внутри ячейки, ячейка может ответить соответствующим образом. Клеткам могут быть даны сигналы расти, метаболизироваться, дифференцироваться в определенные типы или даже умирать.
Синтез ДНК
Нуклеиновая основа аденина является частью аденозина, молекулы, которая образуется из АТФ и помещается непосредственно в РНК. Другие нуклеиновые основания в РНК, цитозине, гуанине и урациле, аналогично образуются из CTP, GTP и UTP. Аденин также обнаружен в ДНК, и его включение очень похоже, за исключением того, что АТФ превращается в форму дезоксиаденозинтрифосфата (dATP), прежде чем стать частью цепи ДНК.
Роль АТФ в энергетическом балансе
АТФ является основной молекулой энергии в живых системах. Он участвует в различных химических процессах, от химического биосинтеза до движения ресничек, сокращения мышц, активного транспорта молекул через клеточную мембрану или распространения электрического импульса через нервные волокна.
Производство и потребление энергии происходит через сеть ферментативных реакций (метаболизм). Центральным химическим соединением в метаболизме является аденозинтрифосфат (АТФ), который образуется в результате метаболических реакций (катаболизм) путем фосфорилирования аденозиндифосфата (АДФ) с образованием энергии около 30 кДж / моль (термодинамика). Большая часть АТФ производится в результате процессов в митохондриях (окислительного фосфорилирования). При использовании этой энергии в биологических процессах АТФ обычно гидролизуется до фосфата и АДФ (аденозинДИфосфата).
Вся биосинтетическая деятельность, как и многие другие клеточные действия, требует энергии. В основном для клеточных активностей источником энергии является именно АТФ. Молекула АТФ состоит из аденина, рибозы и трех фосфатных групп (ФГ). Последние с сильным отрицательным зарядом связаны двумя ковалентными высокоэнергетическими связями, которые при гидролизе выделяют относительно много энергии
Это демонстрирует важное свойство АТФ
Поэтому без преувеличения можно сказать, что наиболее важным энергетическим соединением в клетке является трифосфат аденозина (АТФ), который по своему химическому составу является нуклеотидом.
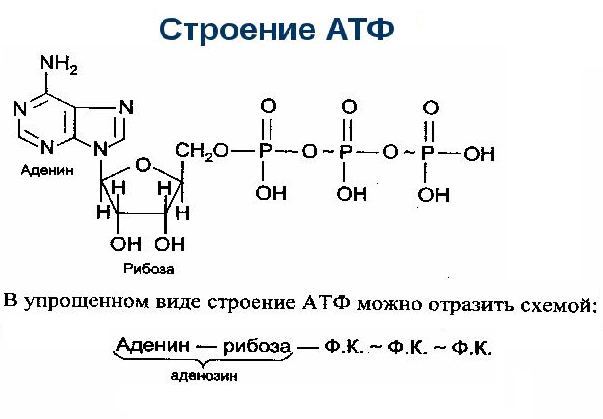
Молекула АТФ состоит из:
- — азотно-аденинового основания пурина;
- — пентозы, рибозы и моносахариды;
- — трех фосфатных групп, обозначенных как альфа, бета и гамма (начиная с рибозы).
Структура АТФ-синтазы
Синтез АТФ состоит из двух частей. Часть, встроенная в мембрану митохондрий (у эукариот), тилакоидную мембрану хлоропласт (только у растений) или плазматическая мембрана (у прокариот) называется ФО. Это двигатель, который питается от ионов H +, протекающих через мембрану. Часть в митохондриях, строма хлоропласта, или внутри бактериального или археального клетка называется F1-ATPase. Это еще один двигатель, который используется для генерации АТФ. Считается, что эти две части были двумя отдельными структурами с двумя различными функциями, которые в конечном итоге превратились в АТФ-синтазу. Область FO похожа на ДНК-геликазы (ферменты, которые распаковывают ДНК, чтобы ее можно было использовать в качестве матрицы для размножения), в то время как область F1-АТФазы похожа на моторы H +, которые позволяют жгутикам, подобным плечевым придаткам, у некоторых бактерий, двигаться. F1-АТФаза имеет центральный стебель и ротор, который при включении преобразует АДФ и Пи в АТФ.
Это рендеринг структуры АТФ-синтазы. FO показан синим и фиолетовым, а F1-АТФаза показана красным.
Синтез АТФ в организме
АТФ чаще всего производится в митохондрии, в основном в результате расщепления глюкозы и жирных кислот в процессе, называемом окислительным фосфорилированием; разложение 1 молекулы глюкозы в митохондрии высвобождает 36 молекул АТФ. Также АТФ синтезируется в хлоропластах, при фотосинтезе в процессе фотосинтетического фосфорилирования.
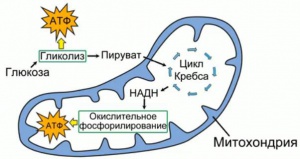
Использование АТФ в клетке
АТФ не может храниться в качестве резерва, поэтому он расходуется после его синтеза путем дефосфорилирования с помощью фермента АТФазы. Две конечные фосфорные группы связаны богатыми энергией ковалентными связями. Когда эти связи разрушаются, высвобождается относительно большое количество энергии. Если от АТФ освободить один конец ФГ, то образуется аденозин дифосфат (АДФ), освободить другой — получится аденозинмонофосфат (АМФ).
Фосфорная группа, высвобождаемая из АТФ или АДФ, богата энергией и, связываясь с соединением, обогащает ее энергией (процесс, называемый фосфорилированием). Таким образом, энергия от АТФ используется в процессах анаболизма.
АТФ создается в качестве основного энергетического продукта процесса разложения пищевых ингредиентов в процессе окисления. Часть энергии, выделяемой в этих процессах, сохраняется в форме АТФ, а остальная часть используется в форме тепла. Полученный таким образом АТФ используется для взаимодействия со всеми типами клеток. Только около 1/3 АТФ расходуется на реакции анаболизма. Остальная энергия расходуется на движение, сокращение мышц, транспортировку вещества через клеточную мембрану и т. д.
Фосфорилирование, регенерация АТФ.
Восстановление (синтез) АТФ реализуется путем связывания ФГ сначала с АМФ, что приводит к АДФ, а затем из АТФ под контролем фермента АТФ-синтазы. Это возможно благодаря тепловым реакциям, в которых энергоемкие (анаболические) реакции связаны с энерговыделительными (катаболическими) реакциями. Энергия, выделяемая при катаболизме, используется для повторного синтеза АТФ из АДФ. Следовательно, система АТФ / АДФ служит универсальным способом обмена энергией, который балансирует между выделяемыми и потребляющими энергию реакциями.
Функциональные характеристики АТФ.
Химическая связь, представляющая собой сумму сил, которые удерживают вместе атомы в молекуле, является стабильной конфигурацией, и для разрыва старой связи и образования новой требуется энергия. Ферменты значительно снижают потребность в активации большого количества энергии, но для того, чтобы химические реакции происходили в живых организмах, необходимо, чтобы энергия связи в продуктах реакции всегда была меньше энергии связи реагентов.
Энергия, выделяемая при удалении фосфатных групп, не только возникает из высокоэнергетических связей, но также является результатом перераспределения орбит в молекулах АТФ или АДФ. Каждая фосфатная группа несет отрицательный заряд и поэтому имеет тенденцию отталкиваться от другой такой группы. Когда фосфатная группа удаляется, происходит изменение конфигурации электронов, в результате чего получается структура с меньшей энергией.
В живых системах АТФ также гидролизуется до АДФ. Гидролиз АТФ является, например, быстрым способом выработки тепла у животных, которые просыпаются от зимней спячки. Однако обычно конечный продукт не просто удаляется, а переносится через фермент (киназу) в другую молекулу (фосфорилирование). Эта реакция также передает часть энергии от высокоэнергетической связи фосфорилированному соединению, которое, таким образом, обогащается энергией при реакции.
Энергия, выделяемая в реакциях клеточного метаболизма, таких как расщепление глюкозы, используется для повторного синтеза АТФ из молекул АДФ. Основными механизмами синтеза АТФ в клетке являются окислительное фосфорилирование в процессе клеточного дыхания (на внутренней стороне митохондриальной мембраны) и фосфорилирование в процессе фотосинтеза.
История создания ATF
Первое трансмиссионное масло под названием ATF-А разработала компания General Motors в 1949 году. До этого, в автоматах использовали моторные масла, и работа коробки была крайне трудной и недолгой.
С развитием автомобилестроения менялись технологии и стандарты. В 1967 году GM ввёл первый стандарт— Dexron type В. Чтобы было легче обнаружить утечку, жидкость окрашивали в красный цвет.
Следующей спецификацией стал Dexron II. Масло обладало слабыми антикоррозионными свойствами: металлические детали АКПП быстро ржавели. К 1990 годам смазку перевели на синтетическую основу.
С появлением в автоматах ЭБУ и гидроблоков требования к маслу ужесточились. GM разработал новые стандарты Dexron III, VI. Совершенствовалась основа, улучшились фрикционные свойства, обновился пакет модификаторов.
General Motors также внедрил спецификацию Allison С4 с требованиями к смазке, работающей в трансмиссиях грузовиков и тяжёлой техники.
Для своих коробок Ford разработал спецификацию М2С33 в 1959 году. А в 1980-х появился стандарт Mercon. Масла, соответствующие требованиям этих спецификаций, схожи по свои характеристикам с Dexron.
Окислительное фосфорилирование
Теперь займёмся окислительным фосфорилированием. Какая была основная суть у катаболизма? Вытащить максимальное количество электронов из молекулы — с этим он отлично справился, если вспомнить катаболизм одной молекулы глюкозы, то в ходе неё были получены 24 электрона — в виде НАДH и ФАДH2. Из них: четыре в гликолизе, четыре в окислительном декарбоксилировании пирувата и шестнадцать в цикле трикарбоновых кислот.
Из одной молекулы глюкозы можно получить 24 электрона.
Зачем это было нужно? Для окислительного фосфорилирования, а если точнее, то одной из его частей — цепи переноса электронов. Мы договорились, что она находится во внутренней мембране митохондрий. Дыхательная цепь состоит из четырёх комплексов, но пока не будем лезть в дебри. Сейчас просто разберёмся с механизмом окислительного фофорилирования.
Четыре комплекса дыхательной цепи и АТФ-синтаза
Электроны, которые были получены в ходе катаболизма, попадают на комплексы дыхательной цепи. Там они перескакивают с одного комплекса на другой, пока не попадут на кислород. В ходе таких перескоков создаётся энергия. Сразу скажу, что её не слишком много. Но достаточно для того, чтобы транспортировать протоны из матрикса в межмембранное пространство. За счёт этого создаётся градиент концентрации протонов. Протоны стараются попасть обратно в матрикс митохондрий, но мембрана для них непроницаема. Так они и бьются в мембрану, пока не попадают на АТФ-синтазу. Можно подумать, что АТФ-синтаза это канал для протонов, но это не совсем так. Транспорт протонов из межмембранного пространства в матрикс создаёт большое количество энергии. Эта энергия используется АТФ-синтазой для синтеза АТФ. Чем-то напоминает
Механизм окислительного фосфорилирования.
Представьте себе шланг. Вода под большим давлением идёт по шлангу, пока не дойдёт до его конца. Чем больше давление в шланге, тем сильнее из него вырывается вода. Примерно такой же принцип в работе окислительного фосфорилирования. Только напор воды создаёт дыхательная цепь, а единственное место выхода для неё — это АТФ-синтаза. Вода — это протоны водорода.
Из этого можно сделать вывод. Если мы не создадим градиент концентрации, то синтеза АТФ не будет. Получается, что работа цепи переноса электронов сопряжена с работой АТФ-синтазы. Это и есть окислительное фосфорилирование. В нём сопряжены три процесса: транспорт электронов по дыхательной цепи, транспорт протонов в межмембранное пространство и синтез АТФ. За первые два процесса отвечает дыхательная цепь, а за последний — АТФ-синтаза. Теперь, когда мы уяснили себе этот принцип, можно лезть в дебри!